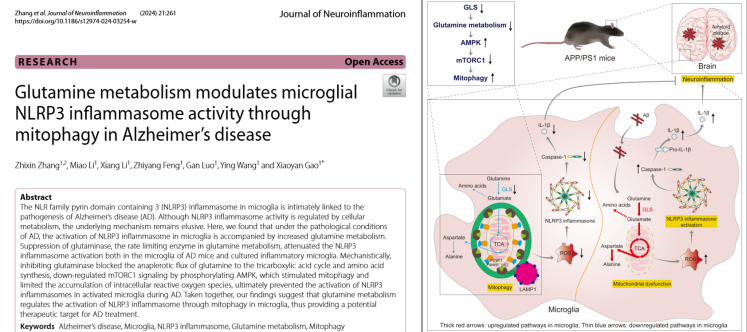
阿爾茨海默病(Alzheimer’s disease, AD)是一種典型的神經退行性疾病,小膠質細胞介導的神經炎癥是其主要病理特征之一。小膠質細胞中NLRP3炎性小體的激活與AD的發病機制密切相關,但其具體活性調控分子機制仍不清楚。北京中醫藥大學高曉燕教授團隊創新性地從AD病理條件下小膠質細胞內代謝重編程與NLRP3炎癥小體之間的關系入手開展谷氨酰胺代謝調控AD神經炎癥全過程機制闡釋,為基于逆轉神經炎癥的AD藥物研發提供新的靶點和思路。
該研究整合代謝組學、代謝流分析及分子生化多種研究方法,發現Aβ能夠激活小膠質細胞中NLRP3炎癥小體,并且在Aβ誘導的NLRP3炎性小體活化小膠質細胞模型中和AD模型小鼠腦內小膠質細胞中的谷氨酰胺代謝顯著增強,而抑制谷氨酰胺限速酶GLS1表達能夠減輕NLRP3炎癥小體活性以及IL-1β和IL-18的產生。進一步研究發現,抑制GLS1酶活性能夠抑制谷氨酰胺回補代謝,阻礙細胞內氨基酸合成,造成細胞營養壓力,誘導線粒體自噬,減少線粒體ROS積累,進而抑制NLRP3炎癥小體激活,最終減輕AD小鼠腦內小膠質細胞介導的神經炎癥反應。該研究相關內容以“Glutamine metabolism modulates microglial NLRP3 inflammasome activity through mitophagy in Alzheimer’s disease”為題發表于中科院一區期刊Journal of Neuroinflammation(https://jneuroinflammation.biomedcentral.com/articles/10.1186/s12974-024-03254-w#article-info)。北京中醫藥大學中藥學院博士后張志新為論文第一作者,高曉燕教授為通訊作者。該項研究工作得到了國家自然科學基金(82104364, U21A20407)和北京市自然科學基金(7222276)的資助。